大B细胞淋巴瘤(LBCL)是最常见的B细胞非霍奇金淋巴瘤,创新的CAR-T疗法在LBCL的治疗中已经占据了不可替代的地位,但目前不少LBCL患者在靶向CD19 CAR-T治疗后面临疾病复发或进展的困境,尤其是伴有高肿瘤负荷、结外受累多、IPI评分高和年龄>65岁等高危因素的患者1-3。对于既往接受靶向CD19 CAR-T治疗失败的患者,现有的治疗手段对患者获益受限。更换靶点的细胞治疗可能是更有效的治疗手段,新型靶向CD20的CAR-T LY007细胞注射液可为伴有高危因素、既往靶向CD19 CAR-T治疗失败的患者提供新的治疗选择。
在备受瞩目的第66届美国血液学会(ASH)年会上,新型靶向CD20 CAR-T细胞治疗产品LY007细胞注射液治疗B细胞非霍奇金淋巴瘤(B-NHL)的临床研究更新数据通过壁报展示的形式公布(Poster 4822)4。医脉通特邀该研究的leading PI上海交通大学医学院附属瑞金医院赵维莅教授及其团队、江苏省人民医院李建勇教授、隆耀生物CMO朱宇翔先生,结合LBCL的治疗现状深入剖析LY007细胞注射液的治疗潜力,以飨读者。
ASH现场直击

该研究的leading PI赵维莅教授与隆耀生物CMO朱宇翔先生
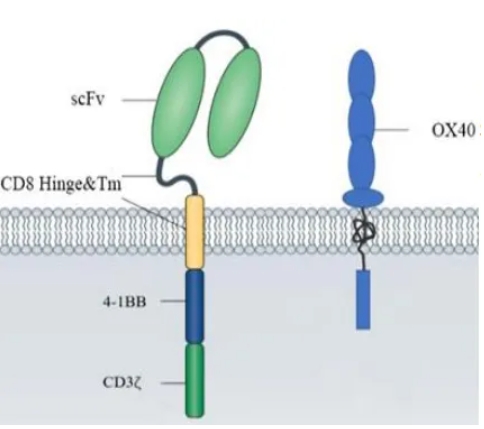
图1 LY007的CAR结构示意图
LY007细胞注射液治疗B-NHL的Ⅰ期临床研究:初步疗效与安全性令人鼓舞
一项单臂、开放、“3+3”剂量递增的Ⅰ期临床研究,探索了新型靶向CD20 CAR-T产品LY007细胞注射液在R/R B-NHL患者中的疗效及安全性,并确定5.0 × 106 cells/kg剂量组进行剂量拓展。
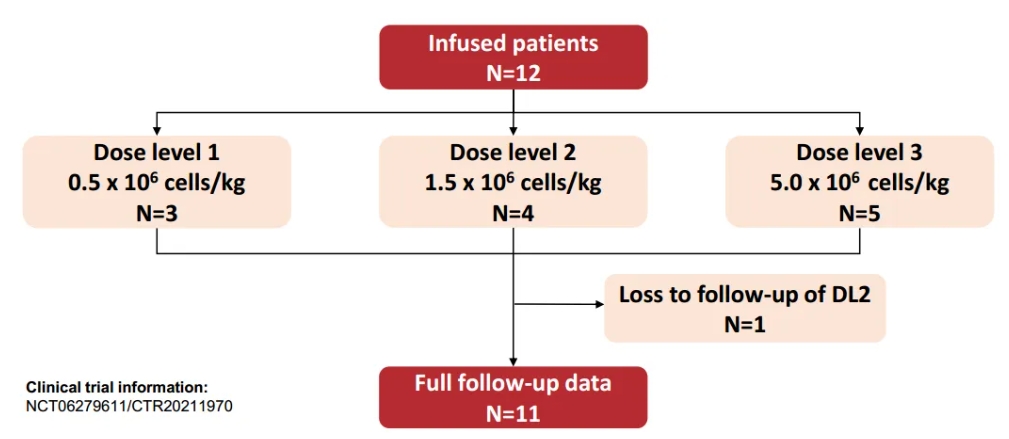
图2 研究设计
表1 基线特征
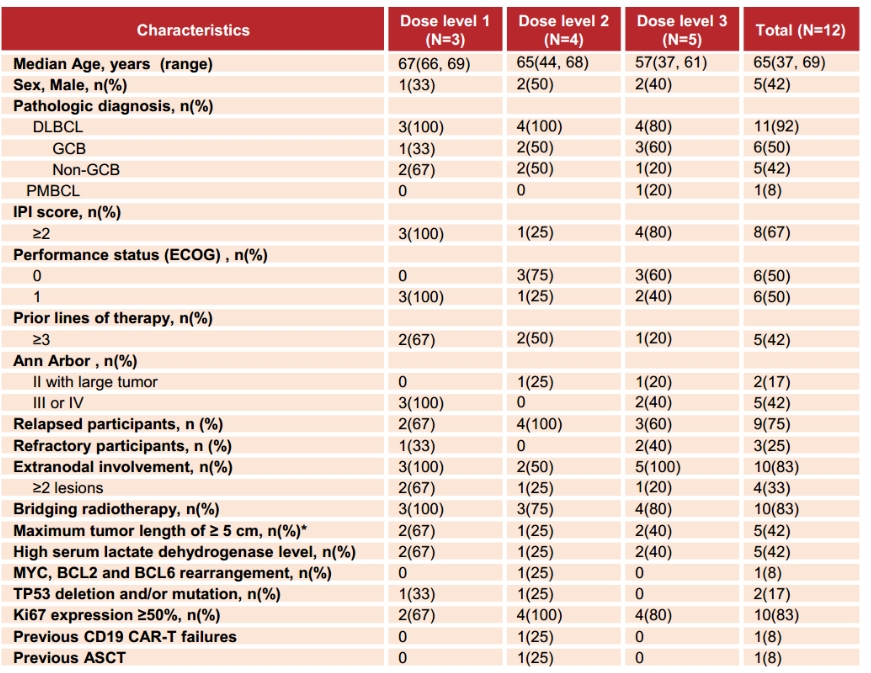
*Two of the subjects had maximum tumor length ≥8 cm.
PMBCL=primary mediastinal B-cell lymphoma.
安全性方面,LY007细胞注射液总体耐受性良好,在研究期间即使剂量水平增加也没有观察到剂量限制性毒性(DLT)、免疫效应细胞相关神经毒性综合征(ICANS)和≥3级细胞因子释放综合征(CRS)。
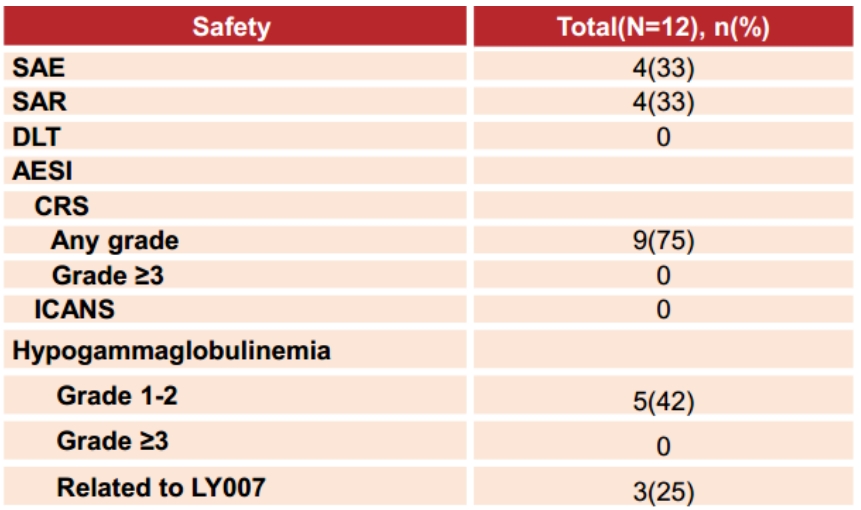
SAE=severe adverse event; SAR= severe adverse reaction; DLT=dose limiting toxicities; AESI=Adverse Event of Special Interest; CRS=cytokine release syndrome; ICANS=immune effector cell-associated neurotoxicity syndrome
在疗效方面,12例患者接受LY007细胞注射液输注后,最佳总缓解率(ORR)为92%,最佳完全缓解率(CRR)为67%,3个月时ORR为73%,CRR为55%。值得注意的是,1例肿瘤长达8.6cm、伴有MYC、BCL2和/或BCL6重排的患者在3个月时达到CR,1例靶向CD19 CAR-T治疗失败和ASCT后复发的患者也在3个月时达到CR。实现缓解的患者可持久缓解,58%的患者缓解持续时间(DoR)超过3个月,有1例患者24个月时依然为CR。缓解也随之转化为生存获益,研究显示中位随访7.2个月时,中位DoR、中位无进展生存期(PFS)和中位总生存期(OS)尚未达到。
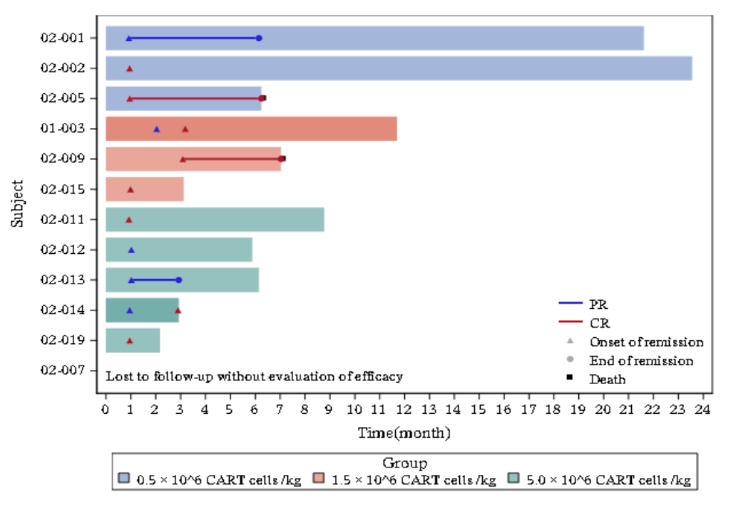
图3 肿瘤评估泳道图
72.7%(8/11)的患者靶病灶SPD变化的最佳百分比较基线下降了50%以上,其中87.5%(7/8)的患者达到CR。在这7例达到CR的患者中,85.7%(6/7)的患者实现了持续缓解。
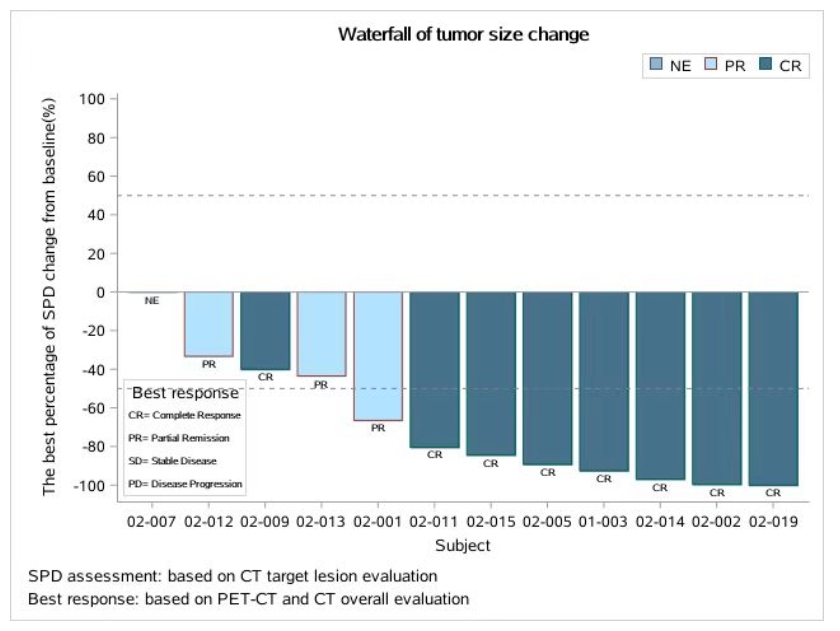
图4 肿瘤大小变化瀑布图
药代动力学(PK)数据显示,3个剂量组的患者都具有良好的CAR-T细胞扩增和长期存续性,尤其DL3组患者外周血中CAR-T细胞峰值中位数为43,200拷贝数/μg DNA,中位第11天达峰,最高平均细胞拷贝数在第11天达到;DL2组患者在第264天时、DL3组患者在第180天时仍可在体内检测到CAR-T细胞。
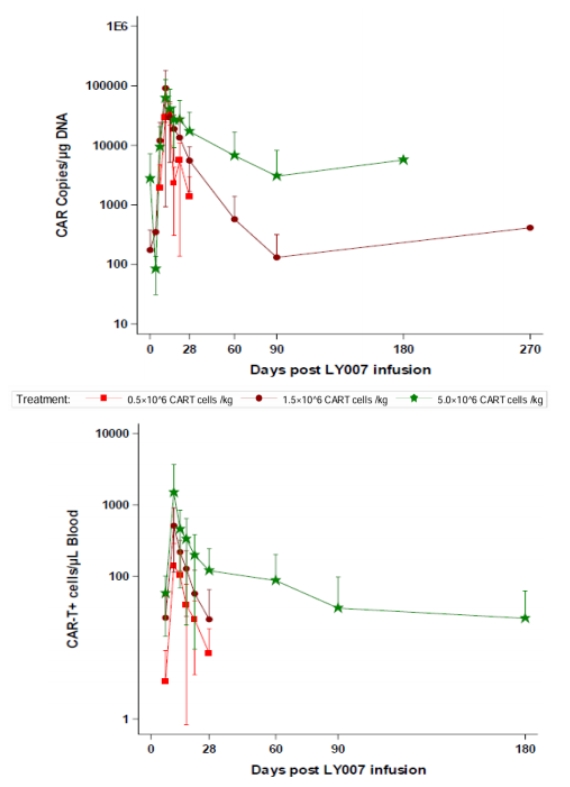
图5 CAR-T细胞扩增和持久性
 李建勇教授
李建勇教授
从此次ASH年会提交的研究摘要可以感受到细胞治疗仍处于蓬勃发展阶段。上海隆耀生物自成立以来致力于肿瘤细胞免疫药物的创新研发,当前已布局CAR-T、UCAR-T细胞疗法等十余条产品管线,覆盖血液肿瘤、实体瘤、自身免疫性疾病等领域,拥有我国首款获批进入注册临床的靶向CD20 CAR-T产品LY007细胞注射液。得益于CD20靶点的差异化选择和OX40共刺激信号分子的创新引入,LY007细胞注射液更进一步满足了目前的临床需求。其OX40共刺激域设计有助于改善肿瘤微环境,有效增强CAR-T细胞的扩增和肿瘤杀伤能力,增强CAR-T细胞的抗耗竭和存续时间。 继今年6月亮相ASCO大会后,LY007细胞注射液再次登上国际学术舞台,此次ASH更新数据涵盖了剂量爬坡和剂量拓展12例受试者的安全性、有效性和药代动力学数据。从有效性上可以观察到,入组患者缓解率高,在疾病缓解深度和抑制肿瘤复发方面也均有显著提升。安全性上,没有发生DLT、ICANS和≥3级的CRS,总体耐受性良好,特别是低丙种球蛋白血症发生率低、发生级别低、持续时间短,可有效提升患者长期生存质量。LY007细胞注射液的出现为临床提供了一种差异化的创新CAR-T疗法,也为靶向CD19治疗无效的患者提供了新的治疗选择。
赵维莅 教授
主任医师,教授,博士生导师 国家杰出青年科学基金获得者 教育部长江学者特聘教授 科技部万人计划领军人才百千万人才工程国家级人选 上海交通大学医学院附属瑞金医院副院长 上海市重中之重临床医学中心主任 上海血液学研究所所长 中华医学会血液学分会副主任委员,淋巴细胞疾病学组组长 中国病理生理学会理事,实验血液学专委会秘书长 中国临床肿瘤协会抗淋巴瘤联盟副主席
盛凌霜 教授
上海交通大学医学院附属瑞金医院 国家转化医学中心(上海) 医学博士 主治医师 作为sub-PI参加多项CAR-T研究的1-2期临床试验 以第一作者及通讯作者身份发表多篇SCI论文 主持及参与国家自然科学基金项目 研究方向:恶性淋巴瘤CAR-T细胞免疫治疗
参考文献:
1. Figura NB, et al. Int J Radiat Oncol Biol Phys. 2021;111(5):1145-1154;
2. Logue, J.M., et al. Curr. Treat. Options in Oncol. 22, 112 (2021).
3. Alarcon Tomas A, et al. Leukemia. 2023;37(1):154-163.
4. 2024 ASH Poster 4822.
5. Ruella M, et al. Nat Rev Drug Discov. 2023;22(12):976-995;
6. Viktoria Blumenberg, et al. Nat Med . 2024 Aug 30
7. Arnon Nagler,et al. How I treat refractory/relapsed diffuse large B-cell lymphomas with CD19-directed chimeric antigen receptor T cells.Br J Haematol . 2023 Mar 14.
8. Mamo T, et al. Clin Chem. 2024 Jan 4;70(1):116-127.
9. Cordas Dos Santos DM, et al.A systematic review and meta-analysis of nonrelapse mortality after CAR T cell therapy.Nat Med . 2024 Jul 8.
10. Tan Su Yin E, Hu YX, Huang H. The breakthrough and the future: CD20 chimeric antigen receptor T-cell therapy for hematologic malignancies. ImmunoMedicine. 2022; 2:e1039.